Il premio Nobel 2017 per la Chimica è stato assegnato a Jacques Dubochet, Joachim Frank e Richard Henderson per aver sviluppato la microscopia crioelettronica per determinare in alta definizione le strutture delle biomolecole.
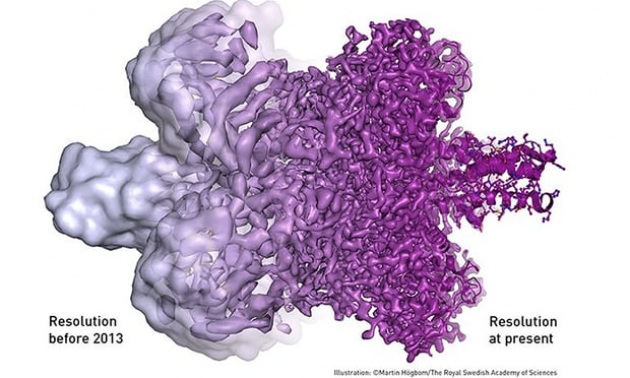
Quest'immagine spiega da sola l'importanza del premio Nobel per la Chimica di quest'anno: a sinistra la risoluzione che avevamo di una biomolecola senza la microscopia crioelettronica. A destra come l'abbiamo con questa tecnica microscopica: molto più definita e dettagliata.|
Si tratta di una tecnica di osservazione al microscopio che rende possibile visualizzare le biomolecole, come le proteine, ma anche il DNA o l'RNA, dopo averle "congelate" molto velocemente, con il metodo della vitrificazione. In questo modo si preserva la loro forma naturale ed è possibile osservare nel dettaglio le relazioni spaziali tra le diverse molecole.
Tecniche come questa hanno rivoluzionato la precisione della microscopia elettronica, che da tecnica utilizzata per vedere ammassi confusi è divenuta un modo per osservare la struttura atomica delle molecole.
Per dare un'idea di quello che la microscopia crioelettronica ha significato per la ricerca basta fare un paragone tra un vecchio televisore con il tubo catodico e un televisore in HD: il tubo catodico è la cristallografia ai raggi X, il televisore in HD è la microscopia crioelettronica.
La tecnica sviluppata grazie alle scoperte dei tre Nobel ha consentito di superare i limiti posti dalle tecniche precedenti, ovvero la cristallografia ai raggi X, sviluppata negli anni '50, la spettroscopia con tecnica di risonanza magnetica, sviluppata negli anni '80.
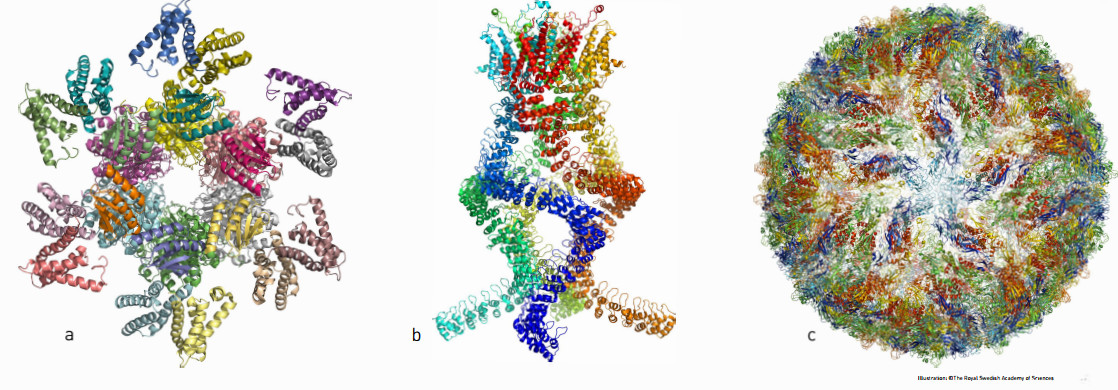
Un esempio di quanto è possibile fare con la tecnica premiata: qui vediamo tre proteine nella loro struttura atomica. La prima è il complesso proteico che governa i ritmi circadiani (una "citazione": è l'argomento del Nobel per la Medicina 2017); la seconda è un sensore di pressione fondamentale per l'udito; la terza è il virus Zika. | The Royal Swedish Academy of Sciences.
Nel 1990 Richard Henderson riuscì a usare un microscopio elettronico per generare un'immagine tridimensionale di una proteina a risoluzione atomica. Questa scoperta dimostrò il potenziale della tecnologia. Joachim Frank ha permesso di rendere applicabile questa tecnologia: tra il 1975 e il 1986 sviluppò un metodo di elaborazione delle immagini in cui le immagini a due dimensioni ricavate dai microscopi vengono analizzate e fuse in modo da svelare la struttura a tre dimensioni delle biomolecole. Jacques Dubochet ha avuto infine il merito di aggiungere l'acqua alla microscopia elettronica. Di norma, l'acqua liquida contenuta nelle cellule evapora nel vuoto di un microscopio elettronico, e questo causa il collasso delle biomolecole che si vogliono analizzare.
D'altro canto, per congelare questa preziosa acqua non si può utilizzare il congelamento lento tradizionale: porterebbe alla formazione di cristalli di ghiaccio che finirebbero col danneggiare le molecole.
Nei primi anni '80, Dubuchet riuscì a vetrificare l'acqua, cioè a congelarla così rapidamente da solidificarla, nella sua forma liquida, attorno a un campione biologico, permettendo alle biomolecole di conservare la loro forma naturale persino nel vuoto.
Questa scoperta ha permesso di sfruttare al massimo le potenzialità della microscopia elettronica. Nel 2013 si è riusciti a raggiungere la tanto agognata risoluzione atomica, e ora i ricercatori riescono a ottenere, come routine, la struttura tridimensionale delle biomolecole. Negli ultimi anni, abbiamo ottenuto immagini precise delle proteine che causano la resistenza antibiotica e della superficie del virus Zika.
Inoltre, la microscopia crioelettronica ha permesso di capire come funzionino le proteine in un contesto dinamico, perché permette di "congelare" i vari stati e poi guardare il quadro complessivo. In futuro, queste informazioni si potranno forse assemblare in una sorta di "film" che riveli che cosa accade, davvero, all'interno delle cellule, comprendendo ogni fotogramma di queste dinamiche.
Al di là delle ovvie ricadute per la biologia di base, questapproccio applicato a proteine di interesse medico permetterà un salto di qualità nella nostra capacità di inventare nuovi vaccini e farmaci.
Un esempio appropriato è la gamma-secretasi che, se mutata, causa lAlzheimer. È in gran parte nascosta allinterno delle membrane cellulari, quindi negli anni ha resistito a molti tentativi di essere visualizzata. Alla fine, ce lhanno fatta proprio per Cryo-EM un paio di anni fa.
Un altro esempio è la recentissima struttura dellinvolucro del virus Zika, pubblicata su Nature. In entrambi i casi, ora le vediamo talmente bene che la speranza è di poter disegnare farmaci che possano aderire esattamente alle loro forme.
Jacques Dubochet è nato nel 1942 a Aigle, in Svizzera. Ha conseguito il dottorato di ricerca allUniversità di Ginevra e allUniversità di Basilea.
Joachim Frank è nato nel 1940 a Siegen, Germania. Dottorato di ricerca allUniversità di Monaco di Baviera oggi insegna alla Columbia University, New York, USA.
Richard Henderson è nato nel 1945 a Edimburgo, in Scozia. Dottorato di ricerca allUniversità di Cambridge, oggi è responsabile del laboratorio di Biologia Molecolare nella stessa università.

focus.it - 6 ottobre 2017